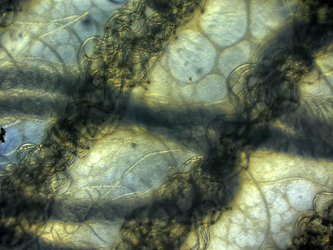
BNC ist die einzige Cellulose, die in Form eines Nanofasernetzwerks aus niedermolekularen Substanzen wie Glukose durch Essigsäurebakterien hergestellt werden kann.
Die Entwicklung von BNC-Produkten mit maßgeschneiderten Eigenschaften zählt zu unseren Kernkompetenzen.
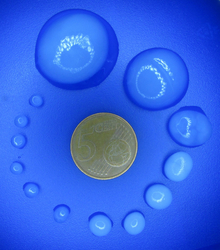
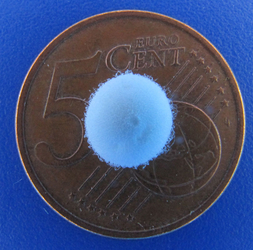
BNC-Kugeln
Durch eine dynamische Kultivierungsmethode lassen sich direkt während der Biosynthese Kugeln mit unterschiedlichen Durchmessern herstellen. Auch hier können zum Kulturmedium Additive verschiedenster Art zugegeben werden, die Einfluss auf die Bildung nehmen.
Sprechen Sie uns an! Gerne entwickeln wir mit Ihnen zusammen neue Produkte.
- dimensionsstabil
- Durchmesser: 1-30 mm
- Zusatz von Additiven möglich
F&E-Leistungen
Suchen Sie nach innovativen Lösungen im Bereich Life Science und Technik?
Sprechen Sie uns an! Gerne entwickeln wir nach Ihren Vorstellungen maßgeschneiderte Produkte!
Wir sind Ihr Berater und Dienstleister bei der Entwicklung und Nutzung von Funktionspolymeren. Mit unserer breitgefächerten und zugleich hochspezialisierten wissenschaftliche Basis, anwendungsorientiertem Wissen und praktischen Erfahrungen unterstützen wir unsere Kunden bei der Vorbereitung serien- und marktorientierter Produktentwicklungen.
Unsere Kernkompetenzen sind synthetische und biosynthetische Polymere.
Wir prüfen Technologien auf ihre Umsetzbarkeit in Produkte und Prozesse, entwerfen Produktkonzepte, bauen Funktionsmuster und helfen Ihnen bei der Entwicklung konkreter, absatzfähiger Produkte.
BNC-Coatings
Mittels MMR-Tech lassen sich eine Vielzahl von Materialien mit BNC beschichten. Diese Coatings mit variablen Schichtdicken entstehen, wenn die BNC nach Ende der Synthese nicht vom Template abgelöst wird. Die Anhaftung und Festigkeit ist abhängig von der Porosität des Templatematerials und kann ebenfalls durch Trocknung beeinflusst werden. Mit diesem Prozess lassen sich beispielsweise Papier, Textilien und Gewebe sowie Medizinprodukte (z.B. aus Keramik) beschichten.
Sprechen Sie uns an! Gerne entwickeln wir mit Ihnen neue Produkte.
BNC-Komposite
Die MMR-Tech ermöglicht das Einbringen von Additiven (gelöst oder dispergiert) während oder nach der Synthese. Im Gegensatz zur stationären Synthese Methode besitzt die MMR-Tech den entscheidenden Vorteil, dass die Additive in jede Schicht der Multischichtsysteme eingelagert werden können und homogen verteilt innerhalb der Matrix vorliegen. Mögliche Additive sind: Aktivkohle, weitere Cellulosetypen (z.B Cellulose-Nanofasern, Carboxymethylcellulose), Alginat (Vernetzung möglich), Wirkstoffe, und viele mehr.
Sprechen Sie uns an! Gerne entwickeln wir für Sie oder mit Ihnen zusammen neue Produkte.
BNC-Fasern
Durch Desintegration von BNC-Formkörpern entstehen Fasern in unterschiedlichen Dimensionen. Durch Zusatz von Additiven während oder nach der Synthese sowie durch post processing (z.B. Trocknungsverfahren) lassen sich die Eigenschaften der Fasern noch weiter beeinflussen.
Sprechen Sie uns an! Gerne entwickeln wir mit Ihnen zusammen neue Produkte.
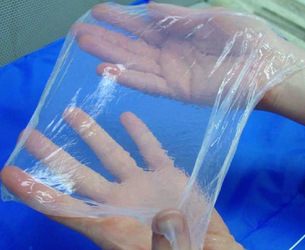
BNC-Membrane
Flächige BNC-Membrane können auf unterschiedliche Weise hergestellt werden. Neben der weit verbreiteten stationären Methode, ermöglicht die MMR-Tech auch hier ein prozessgesteuertes Design funktionsbestimmender Eigenschaften. Hierzu zählen die Oberflächenbeschaffenheiten, die Nanofasernetzwerkarchitektur, und auch ein Mehrschichtaufbau lässt sich mit unserer Methode realisieren.
Maße:
- 200 x 100 x 3 mm (initialfeucht)
- 200 x 100 x 0,03 mm (heißgepresst)
Unsere BNC-Membrane und Hybridmembrane weisen eine prozessgesteuerte Permeabilität für Gase und Flüssigkeiten auf.
- Permeationsrate (Wasserdampf): 14 g.mm/m2.Tag
- Permeationsrate (Sauerstoff): 1,5 N.cm3.mm/m2 Tag.atm
Durch Verwendung von Additiven während oder nach der Biosynthese (siehe auch BNC-Komposite), Trocknungsprozesse und viele weitere Einflussmöglichkeiten, lassen sich die Eigenschaften noch weiter beeinflussen. Durch das wachsende Interesse an nachhaltigen Produkten gelangen BNC-Membrane, ob initialfeucht oder getrocknet, immer mehr in den Fokus von Wissenschaft und Industrie in den Bereichen Verpackungsmaterialien (intelligente, antimikrobielle Verpackungen für Lebensmittel), Elektronik (Biosensoren, Superkondensatoren), Kosmetik (Gesichtsmasken, Ersatz von Mikroplastik in Peelings und Cremes), Medizin (Wundauflagen, Drug Delivery), und viele, viele mehr. In enger Kooperation mit Partnern aus universitären und medizinischen Einrichtungen, haben unsere MMR-Tech Membrane ihren Weg auf den Forschungsmarkt für Drug Delivery Systeme aus Wundauflagen gefunden.
Sprechen Sie uns an! Gerne entwickeln wir für Sie und mit Ihnen zusammen neue, nachhaltige Produkte!
Weiterführende Literatur
Klemm, D.; Petzold-Welcke, K.; Kramer, F.; Richter, T.; Raddatz, V.; Fried, W.; Nietzsche, S.; Bellmann, T.; Fischer, D. BiotechKlemm, D.; Petzold-Welcke, K.; Kramer, F.; Richter, T.; Raddatz, V.; Fried, W.; Nietzsche, S.; Bellmann, T.; Fischer, D. Biotechnanocellulose: A review on progress in product design and today’s state of technical and medical applications. Carbohydr. Polym.2021, 254, 117313.
Alkhatib, Y., Dewaldt, M., Moritz, S., Nitzsche, R., Kralisch, D., & Fischer, D. (2017). Controlled extended octenidine release from a bacterial nanocellulose/poloxamer hybrid system. European Journal of Pharmaceutics and Biopharmaceutics: Official Journal of Arbeitsgemeinschaft Fuer Pharmazeutische Verfahrenstechnik E.V, 112, 164–176.
Karl, B., Alkhatib, Y., Beekmann, U., Bellmann, T., Blume, G., Steiniger, F., et al. (2020). Development and characterization of bacterial nanocellulose loaded with Boswellia serrata extract containing nanoemulsions as natural dressing for skin diseases. International Journal of Pharmaceutics, 587, Article 119635.
Klemm, D., Cranston, E. D., Fischer, D., Gama, M., Kedzior, S. A., Kralisch, D., et al. (2018). Nanocellulose as a natural source for groundbreaking applications in materials science: Today’s state. Materials Today, 21(7), 720–748.
Moritz, S., Wiegand, C., Wesarg, F., Hessler, N., Müller, F. A., Kralisch, D., et al. (2014). Active wound dressings based on bacterial nanocellulose as drug delivery system for octenidine. International Journal of Pharmaceutics, 471(1–2), 45–55.
Müller, A., Ni, Z., Hessler, N., Wesarg, F., Müller, F. A., Kralisch, D., et al. (2013). The biopolymer bacterial nanocellulose as drug delivery system: Investigation of drug loading and release using the model protein albumin. Journal of Pharmaceutical Sciences, 102(2), 579–592.
Müller, A., Zink, M., Hessler, N., Wesarg, F., Müller, F. A., Kralisch, D., et al. (2014). Bacterial nanocellulose with a shape-memory effect as potential drug delivery system. RSC Advances, 4(100), 57173–57184.
Thomas, S., & Pottathara, Y. B. (2020). Nanocellulose based composites for electronics. Elsevier.
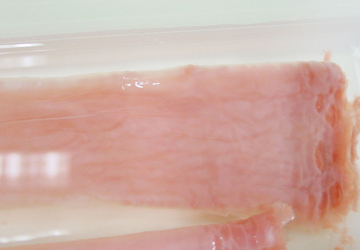
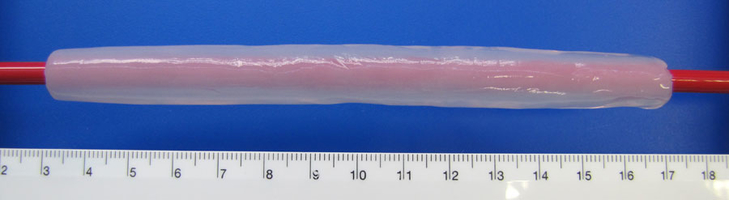
BNC-Tubes
MMR-Tech-Tubes:
Die MMR-Tech ermöglicht die Herstellung beliebig geformter Hydrogelkörper – zum Beispiel in tubulärer Form - direkt während der biotechnologischen Synthese. Ein wesentliches Merkmal dieser Technologie ist, dass Mehrschichtsysteme aufgebaut werden können, und Additive direkt während der Synthese in jede Schicht eingelagert werden können. Die Oberflächen-und Netzwerkstrukturen sowie die Abmessungen der BNC-Tubes sind mit dieser Technologie ebenfalls einstellbar:
- variabler Innendurchmesser: 2,5-30 mm *
- Wandstärken: 1-5 mm *
- Länge bis 175 mm *
- Berstwiderstand: >1100 mbar Innendruck
Trockene MMR-Tech-Tubes:
In post processing Schritten – beispielsweise partielle oder vollständige Trocknung, Laserstrukturierung, Natronlaugeschrumpfung, uvm. – lassen sich die Tubes auch noch nach der Synthese weiter modifizieren und ihre Eigenschaften beeinflussen:
- Durchmesser innen 5 mm
- Wandstärke < 100 µm
- Länge 100 mm
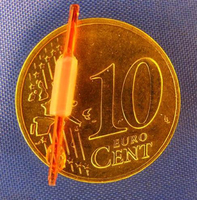
BASYC-Tech-Tubes:
Mit der ebenfalls patentierten BASYC®-Technologie lassen sich Tubes mit besonders kleinem Innendurchmesser herstellen:
- Durchmesser innen 1 mm,
- Durchmesser außen 2,5 mm,
- Länge 10 mm *
* Abmessungen: initialfeucht
Kombiniert man die herausragenden Eigenschaften des Naturpolymers BNC mit dem prozessgesteuerten Design der MMR-Tech, erhält man ein breites Spektrum an Tubes, die insbesondere für medizinische Anwendungen als Implantatmaterialien für den Ersatz von Hohlorganen von großem Interesse sind. Wir besitzen jahrelange Erfahrung im Design von tubulären Implantaten für die Regeneration des Gallengangs und für den Blutgefäßersatz.
Sprechen Sie uns an! Gerne entwickeln wir mit Ihnen zusammen neue Produkte.
Weiterführende Literatur:
GALLENGANGREGENERATION
Klemm, D.O.; Raddatz, V.;Klemm, D.O.; Raddatz, V.;Petzold-Welcke, K.; Kramer, F.; Ruhe,C.; Nietzsche, S.; Settmacher, U.;Rauchfuß, F. Preparation of TubularBiocellulose Implants and Its Use inSurgery—A Review. Processes 2021, 9,2114.
Klemm, D., Rauchfuss, F., Kramer, F., Petzold-Welcke, K., Richter, T., Ruhe, C., & Tannapfel, A. (2016). Design of biocellulose implants for first successful bile duct regeneration. American Chemical Society. 251st ACS National Meeting & Exposition, San Diego, United States.
Rauchfuss, F. (2018). Biocellulosis as scaffold for tissue regeneration in modern surgery. American Chemical Society. 225th ACS National Meeting & Exposition, New Orleans, United States.
Rauchfuss, F., Settmacher, U., Klemm, D., Fried, W., Richter, T., Petzold-Welcke, K., & Ruhe, C. (2017) WO2017021468A1.
KARDIOVASKULÄRE IMPLANTATE
Klemm, D., Ahrem, H., Kramer, F., Fried, W., Wippermann, J., & Kinne, R. W. (2013). Bacterial nanocellulose hydrogels designed as bioartificial medical implants. In M. Gama, P. Gatenholm, & D. Klemm (Eds.), Bacterial nanocellulose: A sophisticated multifunctional material (pp. 175–196). Boca Raton: CRC Press.
Scherner, M., Reutter, S., Klemm, D., Sterner-Kock, A., Guschlbauer, M., Richter, T., Langebartels, G., Madershahian, N., Wahlers, T., & Wippermann, J. (2014). In vivo application of tissue-engineered blood vessels of bacterial cellulose as small arterial substitutes: Proof of concept? The Journal of Surgical Research, 189(2), 340–347.
Schumann, D. A., Wippermann, J., Klemm, D. O., Kramer, F., Koth, D., Kosmehl, H., Wahlers, T., & Salehi-Gelani, S. (2009). Artificial vascular implants from bacterial cellulose: Preliminary results of small arterial substitutes. Cellulose, 16(5), 877–885.
Wacker, M., Kießwetter, V., Slottosch, I., Awad, G., Paunel-Görgülü, A., Varghese, S., Klopfleisch, M., Kupitz, D., Klemm, D., Nietzsche, S., Petzold-Welcke, K., Kramer, F., Wippermann, J., Veluswamy, P., & Scherner, M. (2020). Hemo- and cytocompatibility of surface modified bacterial nanocellulose small diameter vascular grafts: an in vitro study. PLOS ONE.
Weber, C., Reinhardt, S., Eghbalzadeh, K., Wacker, M., Guschlbauer, M., Maul, A., Sterner-Kock, A., Wahlers, T., Wippermann, J., & Scherner, M. (2018). Patency and in vivo compatibility of bacterial nanocellulose grafts as small-diameter vascular substitute. Journal of Vascular Surgery, 68(6S), 177S-187S.e1.