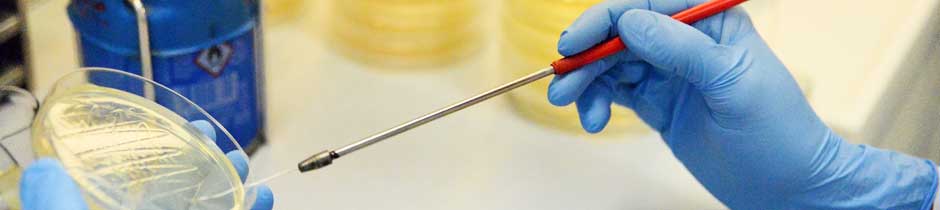
MMR-Tech-Tubes:
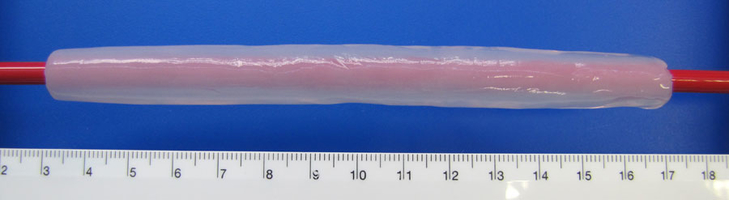
Die MMR-Tech ermöglicht die Herstellung beliebig geformter Hydrogelkörper – zum Beispiel in tubulärer Form - direkt während der biotechnologischen Synthese. Ein wesentliches Merkmal dieser Technologie ist, dass Mehrschichtsysteme aufgebaut werden können, und Additive direkt während der Synthese in jede Schicht eingelagert werden können. Die Oberflächen-und Netzwerkstrukturen sowie die Abmessungen der BNC-Tubes sind mit dieser Technologie ebenfalls einstellbar:
- variabler Innendurchmesser: 2,5-30 mm *
- Wandstärken: 1-5 mm *
- Länge bis 175 mm *
- Berstwiderstand: >1100 mbar Innendruck
Trockene MMR-Tech-Tubes:
In post processing Schritten – beispielsweise partielle oder vollständige Trocknung, Laserstrukturierung, Natronlaugeschrumpfung, uvm. – lassen sich die Tubes auch noch nach der Synthese weiter modifizieren und ihre Eigenschaften beeinflussen:
- Durchmesser innen 5 mm
- Wandstärke < 100 µm
- Länge 100 mm
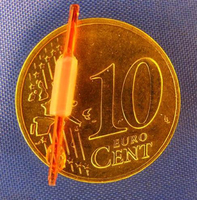
BASYC-Tech-Tubes:
Mit der ebenfalls patentierten BASYC®-Technologie lassen sich Tubes mit besonders kleinem Innendurchmesser herstellen:
- Durchmesser innen 1 mm,
- Durchmesser außen 2,5 mm,
- Länge 10 mm *
* Abmessungen: initialfeucht
Kombiniert man die herausragenden Eigenschaften des Naturpolymers BNC mit dem prozessgesteuerten Design der MMR-Tech, erhält man ein breites Spektrum an Tubes, die insbesondere für medizinische Anwendungen als Implantatmaterialien für den Ersatz von Hohlorganen von großem Interesse sind. Wir besitzen jahrelange Erfahrung im Design von tubulären Implantaten für die Regeneration des Gallengangs und für den Blutgefäßersatz.
Sprechen Sie uns an! Gerne entwickeln wir mit Ihnen zusammen neue Produkte.
Weiterführende Literatur:
GALLENGANGREGENERATION
Klemm, D.O.; Raddatz, V.;Klemm, D.O.; Raddatz, V.;Petzold-Welcke, K.; Kramer, F.; Ruhe,C.; Nietzsche, S.; Settmacher, U.;Rauchfuß, F. Preparation of TubularBiocellulose Implants and Its Use inSurgery—A Review. Processes 2021, 9,2114.
Klemm, D., Rauchfuss, F., Kramer, F., Petzold-Welcke, K., Richter, T., Ruhe, C., & Tannapfel, A. (2016). Design of biocellulose implants for first successful bile duct regeneration. American Chemical Society. 251st ACS National Meeting & Exposition, San Diego, United States.
Rauchfuss, F. (2018). Biocellulosis as scaffold for tissue regeneration in modern surgery. American Chemical Society. 225th ACS National Meeting & Exposition, New Orleans, United States.
Rauchfuss, F., Settmacher, U., Klemm, D., Fried, W., Richter, T., Petzold-Welcke, K., & Ruhe, C. (2017) WO2017021468A1.
KARDIOVASKULÄRE IMPLANTATE
Klemm, D., Ahrem, H., Kramer, F., Fried, W., Wippermann, J., & Kinne, R. W. (2013). Bacterial nanocellulose hydrogels designed as bioartificial medical implants. In M. Gama, P. Gatenholm, & D. Klemm (Eds.), Bacterial nanocellulose: A sophisticated multifunctional material (pp. 175–196). Boca Raton: CRC Press.
Scherner, M., Reutter, S., Klemm, D., Sterner-Kock, A., Guschlbauer, M., Richter, T., Langebartels, G., Madershahian, N., Wahlers, T., & Wippermann, J. (2014). In vivo application of tissue-engineered blood vessels of bacterial cellulose as small arterial substitutes: Proof of concept? The Journal of Surgical Research, 189(2), 340–347.
Schumann, D. A., Wippermann, J., Klemm, D. O., Kramer, F., Koth, D., Kosmehl, H., Wahlers, T., & Salehi-Gelani, S. (2009). Artificial vascular implants from bacterial cellulose: Preliminary results of small arterial substitutes. Cellulose, 16(5), 877–885.
Wacker, M., Kießwetter, V., Slottosch, I., Awad, G., Paunel-Görgülü, A., Varghese, S., Klopfleisch, M., Kupitz, D., Klemm, D., Nietzsche, S., Petzold-Welcke, K., Kramer, F., Wippermann, J., Veluswamy, P., & Scherner, M. (2020). Hemo- and cytocompatibility of surface modified bacterial nanocellulose small diameter vascular grafts: an in vitro study. PLOS ONE.
Weber, C., Reinhardt, S., Eghbalzadeh, K., Wacker, M., Guschlbauer, M., Maul, A., Sterner-Kock, A., Wahlers, T., Wippermann, J., & Scherner, M. (2018). Patency and in vivo compatibility of bacterial nanocellulose grafts as small-diameter vascular substitute. Journal of Vascular Surgery, 68(6S), 177S-187S.e1.